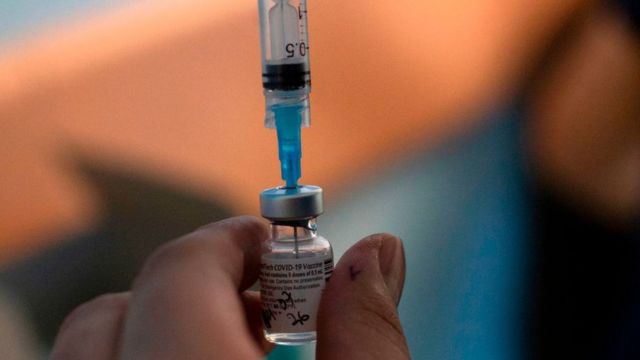
La Administración de Fármacos y Alimentos (FDA, por su sigla en inglés) de Estados Unidos aprobó el uso de emergencia de un medicamento para prevenir el contagio por coronavirus destinado a quienes por su condición médica no pueden ponerse una vacuna.
Se espera que las primeras dosis del medicamento de AstraZeneca, una combinación de anticuerpos de acción prolongada (ACAP), estén disponibles muy pronto.
La vacuna se usará en adultos y adolescentes (de 12 o más años que pesen 40 kg o más) con compromiso inmunitario debido a una condición médica o medicamentos inmunosupresores que pueden no tener una respuesta inmune adecuada a la vacunación contra el COVID-19.
Así como aquellas personas para las que no se recomienda la vacunación contra el COVID-19.
Las personas que lo reciban no deben estar actualmente infectados o haber tenido una exposición conocida reciente a una persona infectada con SARS-CoV-2.
Evusheld es una combinación de dos anticuerpos monoclonales de acción prolongada y es la única terapia de anticuerpos autorizada en los Estados Unidos para prevención.
También es el único anticuerpo contra COVID-19 administrado por vía intramuscular (150 mg de tixagevimab y 150 mg de cilgavimab).
Se están realizando estudios para proporcionar información sobre el impacto de la nueva variante Ómicron (B.1.1.529) en Evusheld.
AstraZeneca acordó suministrar al gobierno de los Estados Unidos 700,000 dosis de Evusheld. Mientras que el gobierno estadounidense indicó que planea distribuir estas dosis prorrata y sin costo a estados y territorios.